深度咨询报告。
儿童是祖国的未来,儿童用药的可及性一直备受国家有关部门、医药行业及社会各界的广泛关注。
儿童有别于成人,其器官功能尚未发育完全,肝脏解毒和肾脏排泄等功能较弱,因此对药物的耐受性较差,如果用药不当,很容易引起不良反应/事件,甚至对健康造成超过疾病本身的严重危害。这使得儿童药的研发相对于成人,研发成本更高、研发难度更大、临床风险也更高。很多医药企业为了规避风险,不太愿意进行儿童药的开发,使得儿童用药长期处于“缺医少药”的困境。
我国儿童用化药产品现状
据国元证券报告数据,2016年到2021年,中国儿童药市场规模由650亿元增长至1080亿元,年均复合增长率为10.69%。据药智咨询分析整理,在我国儿童用药市场中,化学药占主导地位,约2400种,约占整体市场的65%;生物药及中药约占35%。而在儿童用化药中,儿童专用化药仅占儿童化药的5%左右,其余近95%为儿童兼用化药(儿童兼用化药指既可用于成人,也可用于儿童的药品),儿童专用药用药缺口之大,几乎不言而喻。

图1国内上市儿童化药分布情况
数据来源:药智数据,药智咨询整理
在约2400种儿童化药中,剂型主要集中在片剂、注射剂及胶囊剂,这三种剂型的占比达到了73%。产品规格上,约90%的产品都只有一种规格,而对于儿童来说,适应性更高的口服溶液剂、混悬剂等却不到10%。
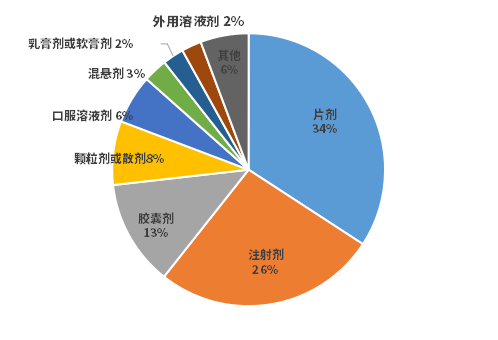
图2国内上市儿童化药剂型分布情况
数据来源:药智数据,药智咨询整理
适应症方面,过于集中在抗感染、营养素补充剂和镇痛药三大类别。据《国家药品不良反应监测年度报告(2022年)》数据显示[1],儿童用化学药中,抗感染药和呼吸系统用药的不良反应比例高于该类别药品在化学药总体不良反应报告中的比例,提示儿童患者使用抗感染药和呼吸系统用药较多,不良反应发生情况也较多。

图3国内上市儿童化药适应症分布情况
数据来源:药智数据,药智咨询整理
从我国儿童用化药产品分布情况可以看出,目前我国儿童用药处于“三少两多一差”的局面,即儿童专用药品种少、剂型少、规格少,儿童普通疾病用药多、不良反应多,用药依从性差。
正是由于我国儿童专用药少、可灵活分剂量的剂型少及产品规格少,很多患儿在服药时都被当成“缩小版的成人”对待,按照“小儿酌减”的原则服用成人药,导致使用上长期存在“用药靠掰,剂量靠猜”,“小儿酌减”情况。
一项某儿童医院超说明书用药情况调查数据结果显示:在调查的2514张有效处方中,含医嘱7159条,涉及264种药品,超说明书用药发生率按处方数为57.24%,按医嘱条数为27.34%。主要超说明书的类型为未提及儿童用药信息(57.23%)和超适应证或功能主治(25.86%)[2]。
可以说,我国儿童药约等同于短缺药。
儿童药短缺原因何在?
儿童药变成短缺药,究其原因,主要有以下几点:
(1)临床试验开展难
儿童临床试验的开展主要包括儿童患者的招募、儿童伦理、临床试验方案设计、临床试验实施等。
患者招募难。作为监护人,家长有保护孩子的本能和责任感,他们害怕孩子作为“试验动物”受到伤害。因此,多数情况下家长倾向于拒绝儿童进行药物临床试验,这就导致儿童患者招募难。同时儿童相对于成人人口体量更小,对于一些儿童罕见病,其患者的招募更是难上加难。
儿童伦理难。儿童伦理是儿童临床试验开展中一项非常复杂的工作,其中包括知情同意理解、伦理保险、伦理受益等,这些都需要与医院、受试者及家人充分沟通。而且目前儿童的经济补偿饱受争议,付费的儿科临床试验会影响家长和受试儿童本身的决策;而不补偿受试儿童相应的损失又可能会给其造成不必要的经济负担。
儿童临床试验方案设计难。儿童临床试验需要在遵循良好的临床研究设计原则和法规要求的基础上,通过充分利用现有数据,尽量减少儿科受试人群的数量和研究步骤。但儿童身体尚未发育完全,同时存在个体发育差异,这使得儿童用药剂量的确定及剂量爬坡比较困难,同时,由于儿科人群与成人的差异,评价药物治疗效果的临床终点或生物标志物也可能存在差异,因此主要疗效指标/次要疗效指标也很难确定。
临床试验实施难。临床试验中儿童用药依从性较差,具体包括服药、检查、饮食、生活方式等。临床试验中儿童依从性与成人不同,不仅仅是患儿,家长也是需要考虑的对象,因为给药等行为通常都是由家长主导完成的。除此之外,药品口味不佳也会导致儿童拒绝或减少服用,导致临床试验实施难度加大,药品的安全性及有效性评估也容易产生偏差。
(2)安全性、有效性与依从性之间难平衡
在保证儿童用药安全、有效的前提下,提高儿童用药的依从性成为一个挑战。
大多数药品的口味、外观并不讨喜,使得很多儿童患者不愿意服用,而通过加入药物辅料,如矫味剂、香精、色素、防腐剂后,其口味、外观能得到改善,但随之带来的问题就是辅料的加入对药品安全性的影响,这使得儿童药的处方设计更加困难。
(3)相较于成人用药,儿童药体量较小
据药智咨询分析统计,目前我国儿童常见疾病主要为呼吸系统(抗感染)及消化系统疾病(腹泻),见表1。然而,目前这两类疾病上市品种较多,市场竞争激烈,很难从中突破。对于一些发病率低的疾病(如白血病、儿童肿瘤、儿童罕见病),一方面要解决研发难题及研发失败带来的风险,另一方面又要考虑产品上市后销售额是否能填补研发投入费用并获得经济收益,而为了避免收益和投入的倒挂,企业对于儿童低发病率疾病药物的研发往往持谨慎态度。
表1我国儿童高发疾病及流行病学数据

*数据来源:全球疾病负担数据库,药智咨询整理
政策支持+市场空白
催生儿童药蓝海市场
法规是医药行业的第一生产力。
美国、日本、欧盟早在2000年以前就发布了儿童药相关法规、指南,美国更是通过立法强制进行儿童药物研究。
中国起步相对较晚,自2011年才开始发布《中国儿童发展纲要(2011-2020年)》,2014年发布我国儿科用药的首个综合性指导文件—《关于保障儿童用药的若干意见》。
近年来,我国又相继发布了多项儿童药相关政策,如发布《鼓励研发申报儿童药品清单》、设立儿童药专栏及发布多种儿童药研发指导原则;如国家医保目录调整方案将儿童药物列为优先考虑调入药品、《国家基本药物目录管理办法(修订草案)》征求意见稿中首次提出将儿童用药作为目录单列等。
我国儿童药在研发、审评审批、市场准入等方面都得到政策大力支持。
据国家统计局发布的最新数据显示,我国0~14岁人口数为24678万,约占总人口的17.5%。然而,目前我国儿童用药市场规模仅占整个医药行业的5%,儿童用药市场远未饱和。
另一方面,根据国家卫健委公布数据,0~14岁儿童两周患病率与就诊率均有所上升,其中0~4岁儿童两周患病率由2008年的17.4‰提升至2018年的22‰;5-14岁儿童两周患病率由2008年的7.7‰提升至2018年的13.1‰。随着三胎政策的放开,儿童药需求将得到持续提升。在政策支持及日益旺盛的儿童药市场需求下,我国儿童药发展也将步入快车道。
而如何使步入儿童药快车道上的企业走得又快又好,需要国家相关部门、医药企业及儿科专业人才的紧密沟通交流及合作,未来可以朝着以下几点努力:
(1)在国家政策层面,儿童药法规体系还不够完善,目前政策大多集中在鼓励研发端,实际上,儿童药的发展需要在药品生命周期各个环节同时进行政策发力[3]。如借鉴美国通过立法强制进行儿童药物研究,企业提交新药申请时,必须提供儿科临床研究计划群体的安全性和有效性评价资料;借鉴日本实行独特的药品定价制度对儿童药研发进行价格激励,比如对儿童药进行价格加算[3]。
(2)从研发资金的支持上,加大对儿童用药研究的资金扶持力度。如成立“儿科创新药研发支持基金”、科技重大专项单列儿科创新药研发支持计划[4]、企业研发并成功上市一款儿童药给予一定的奖励费用等。
(3)从人才培养及平台搭建上,政府可以加大对现有儿科专业人才的扶持,提高其福利待遇,高校可以进一步深化儿科方向的本科和研究生的培养、单独开设儿科临床医学专业并扩大专业的招生规模,来强化我国儿科专业人才体系的建设[4];同时建议成立专业的儿童伦理委员会及医院—企业端临床未满足需求沟通桥梁,缩短临床及研发端的时间差。
结语
总的来说,由于儿童药的研发难度相较于成人更大,很多药企不愿意开发儿童药,导致目前我国儿童药市场“缺药”问题相当严峻。国家为了保障儿童用药的可及性,近几年出台了各项政策大力支持儿童药的研发,儿童药迎来了久违的“春天”。
未来,在临床未满足需求及更多儿药政策的持续推动下,那些选择在“春天”播种儿药的企业,也将会在“秋天”收获儿药市场的红利。
参考文献
[1]《国家药品不良反应监测年度报告(2022年)》
[2]李天姿,金彦,唐淑含.某儿童医院门诊超说明书用药情况调查分析.中国药学杂志.2022,57(23),2030-2034.
[3]李新宇,邵蓉,白铭钰等人.我国儿童药保障政策文本量化分析.中国卫生政策研究.2022年8月第15卷第8期.
[4]钟一鸣,张天义,郭文.中美儿科临床试验管理的比较研究.中国新药杂志.2021年第30卷第14期.
声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智咨询立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请点击右侧在线咨询反馈。
 产业与战略研究
产业与战略研究 品类与产品规划
品类与产品规划 研发与投资决策
研发与投资决策 卓越上市策划
卓越上市策划 成熟产品策划
成熟产品策划
想了解更多报告信息
请扫描二维码联系我们

想了解更多报告信息
请扫描二维码联系我们

想了解更多报告信息
请扫描二维码联系我们

想了解更多报告信息
请扫描二维码联系我们

想了解更多报告信息
请扫描二维码联系我们

想了解更多报告信息
请扫描二维码联系我们
