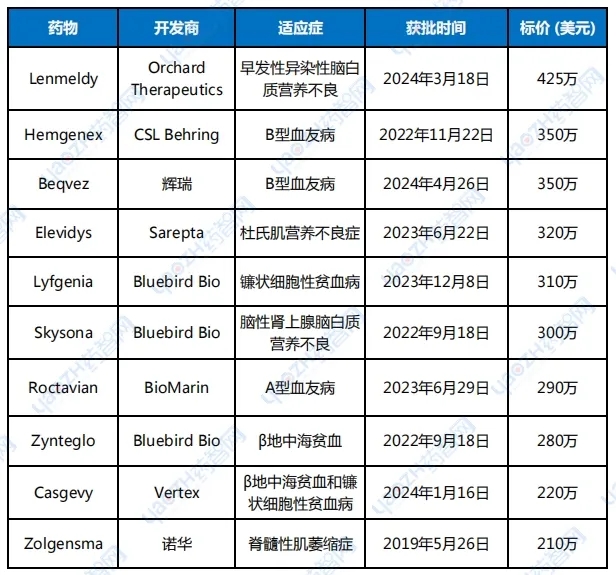
医药领域正在经历一个药价纪录“日日新”的时代,最高药价不断被新批准的疗法刷新。从平均疗法价格来看,基因疗法无疑显著高于其它模式,无论是CAR-T还是其它细胞疗法,其平均价格都难以望其项背。值得注意的是,近期巴西与印度针对基因疗法的降价动作不断,试图改变天价药物现状。巴西、印度能成为“救火队员”吗?据统计,标价排名前十位的基因疗法价格都超过了200万美元。尽管许多先进疗法具有显著的临床益处,但其成本效益仍然令人担忧。
临床和经济审查研究所对多种先进疗法产品进行了分析,结果是制造商的定价普遍高于合理价格。例如,考虑到潜在的成本抵消,ICER建议Hemgenix的价格基准为290万美元(实际成本为350万美元),Zolgensma的价格基准为110至210万美元(实际标价为210万美元),Zynteglo的具有成本效益价格为210万美元,而实际价格为280万美元。《自然》2023年发表的一份报告指出,细胞和基因疗法的年成本平均为204亿美元。该报告预计,2026年年度支出将增至253亿美元,但在2034年将下降至210亿美元。
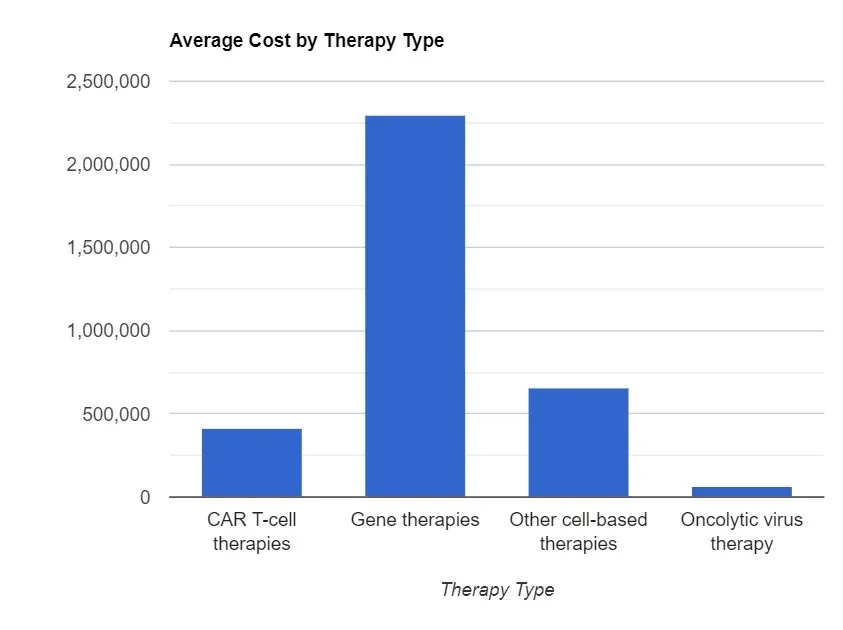
图片来源:Drug Discovery&Development
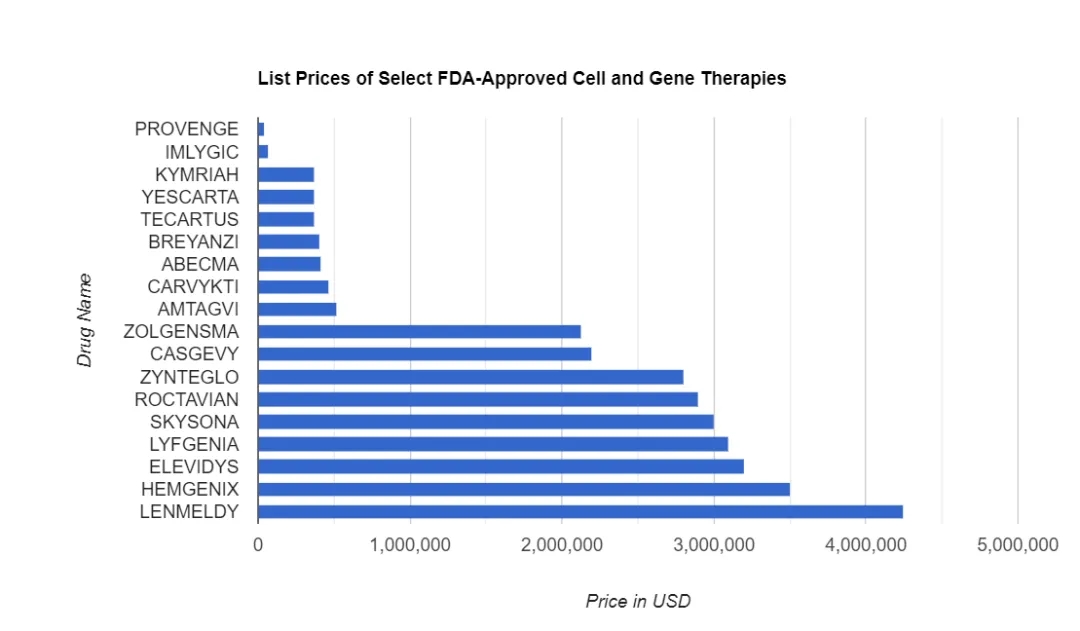
图片来源:Drug Discovery&Development尽管人们普遍认为,基因和细胞疗法相对于终生治疗来说具有成本效应,但高昂的价格仍然是行业内关注的焦点,迫切需要降低细胞和基因疗法的天价,使得这些“此曲只应天上有”的药物尽快恩泽众生。目前,巴西正试图通过美国非营利组织Caring Cross,以及由巴西卫生部资助的公共卫生和研究基金会Fiocruz之间的独特合作伙伴关系来做到这一点。Caring Cross认为,通过提供自己的设备和专业知识,政府和患者应该能够节省大量资金。Caring Cross和Fiocruz之间的合作目标是在巴西本地制造细胞和基因疗法,针对包括白血病、淋巴瘤和艾滋病毒感染的CAR-T细胞疗法。巴西方面的倡议最初侧重于CAR-T疗法,向巴西公共卫生系统收取每剂约3.5万美元的费用。这大约是美国和欧洲目前批准的CAR-T细胞产品价格的十分之一。同其它模态的药物不同,先进疗法的成本中制造费用占据相当显著的比例。与之形成对比的是,每月价格1000美元左右的Wegovy,其生产成本据称不足5美元,而且最大来源还是注射笔。正是考虑到基因和细胞疗法成本中制造费用的显著贡献,人们才认为在海外生产将大幅降低这些昂贵药物的价格。Caring Cross开发的制造工艺可显著降低制造CAR-T细胞治疗产品的材料成本。这家非营利组织将向Bio-Manguinhos(负责生产疫苗、诊断产品和生物制剂的Fiocruz部门)提供技术、材料和培训,以便其能够生产CAR-T细胞疗法和载体。计划是对实验疗法进行临床试验,然后在巴西寻求批准。Caring Cross方面称,首批研究预计将于今年或2025年初开始,批准的产品可能会在三年内上市。除了材料和培训之外,Caring Cross还将向医院提供专有载体,作为生产和治疗的关键材料。印度的生物技术公司,包括ImmunoACT和Immuneel,正在致力于开发负担得起的CAR-T疗法。即使在欧洲,特殊政策也使得一些医院能够生产自己的CAR-T疗法。据称西班牙巴塞罗那医院诊所开发的一种CAR-T疗法获得了西班牙监管机构的批准,并由国家卫生系统报销,为患者提供了另一种选择,价格为8.9万欧元(9.7万美元),大约是生物制药公司市场上CAR-T产品标价的三分之一。Caring Cross与Fiocruz之间的合作估计将接受2000名患者,每位患者的费用在3.5万到4万美元之间,总成本只有7000万美元,而按照目前的标价则为7亿美元。Caring Cross预计今年到明年开始淋巴瘤和白血病疗法临床试验。这些疗法最初将用于三线治疗,但之后会考虑二线治疗,这将显著扩大应用范围。同印度的合作有所不同,Caring Cross将为ImmunoACT提供载体,后者已经开始销售CAR-T疗法,但已经开始着手下一代产品。ImmunoACT目前以约4万美元的价格出售一种疗法,但只有富人才能负担得起。ImmunoACT希望用Caring Cross材料制成的新疗法能够惠及更多患者。印度目前有大约2.5万到3万人有资格接受ImmunoACT开发的CAR-T产品,但只有2千到5千人能够承担治疗费用。ImmunoACT首席执行官称,目前的计划是向富裕患者收取4万美元,而对其它患者收取3万美元。为了扩大覆盖范围,ImmunoACT希望说服政府提高保险覆盖范围。细胞和基因疗法的潜在变数包括治疗效果的持久性、特定的患者群体以及替代疗法的可用性,这些都会显著影响成本效益的计算。例如BioMarin的A型血友病基因疗法Roctavian(valoctocogene roxaparvovec)2024年第一季度收获了80万美元的销售额,而BioMarin原本视其为潜在的重磅炸弹。Roctavian针对的是个存在着激烈竞争的市场。患者不仅疗法选择不少,而且价格体系也具有足够的差异性,患者和付款人可能更不愿意尝试新的昂贵的替代方案。替代疗法的可用性,即使效果较差,也将提高新基因疗法的成本效益的门槛高度。随着更多长期数据的出现,细胞和基因疗法是否能够实现其临床承诺,证明其高昂的成本是合理的,将在未来几年变得更加清晰。治疗效果的持久性仍然是一个关键考虑因素。对于先进疗法高价格的一个常见背书是,这些具有终生效果的一次性疗法比需要重复给药的疗法更具成本效益。然而如果这个基础不存在,那么高价便成为了“空中楼阁”。患者群体的规模是另一个重要因素。与更常见疾病的治疗相比,罕见病和超罕见疾病疗法在收回开发成本方面面临着更严峻的挑战,这是由患者群体的数量和可及性决定的。总而言之,先进疗法的推广,需要尽快降低成本,验证其安全性和长期有效性。通过这些手段,这些疗法的市场占有率才能得到显著提升。
声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智咨询立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请点击右侧在线咨询反馈。
1.Shah-Neville,W.Can Brazil make cell and gene therapy costs affordable for all?Labiotech.29.04.2024.2.Buntz,B.With prices topping$4 million,high stakes define cell and gene therapy landscape.Drug Discovery&Development.26.04.2024.3.Silverman,E.A nonprofit does deals in Brazil and India to make low-cost CAR-T cell therapies widely available.STAT.08.05.2024.4.Wong,C.H.et al.The estimated annual financial impact of gene therapy in the United States.Gene Ther 30,761–773(2023).https://doi.org/10.1038/s41434-023-00419-9
医药领域正在经历一个药价纪录“日日新”的时代,最高药价不断被新批准的疗法刷新。从平均疗法价格来看,基因疗法无疑显著高于其它模式,无论是CAR-T还是其它细胞疗法,其平均价格都难以望其项背。值得注意的是,近期巴西与印度针对基因疗法的降价动作不断,试图改变天价药物现状。巴西、印度能成为“救火队员”吗?01天价基因疗法们据统计,标价排名前十位的基因疗法价格都超过了200万美元。尽管许多先进疗法具有显著的临床益处,但其成本效益仍然令人担忧。表1 基因疗法价格排名表数据来源:公开资料整理临床和经济审查研究所对多种先进疗法产品进行了分析,结果是制造商的定价普遍高于合理价格。例如,考虑到潜在的成本抵消,ICER建议Hemgenix的价格基准为290万美元(实际成本为350万美元),Zolgensma的价格基准为110至210万美元(实际标价为210万美元),Zynteglo的具有成本效益价格为210万美元,而实际价格为280万美元。《自然》2023年发表的一份报告指出,细胞和基因疗法的年成本平均为204亿美元。该报告预计,2026年年度支出将增至253亿美元,但在2034年将下降至210亿美元。图1 先进疗法平均价格对比图图片来源:Drug Discovery&Development图2 细胞与基因疗法价格图图片来源:Drug Discovery&Development02巴西、印度,能成为“救火队员”吗?尽管人们普遍认为,基因和细胞疗法相对于终生治疗来说具有成本效应,但高昂的价格仍然是行业内关注的焦点,迫切需要降低细胞和基因疗法的天价,使得这些“此曲只应天上有”的药物尽快恩泽众生。目前,巴西正试图通过美国非营利组织Caring Cross,以及由巴西卫生部资助的公共卫生和研究基金会Fiocruz之间的独特合作伙伴关系来做到这一点。Caring Cross认为,通过提供自己的设备和专业知识,政府和患者应该能够节省大量资金。Caring Cross和Fiocruz之间的合作目标是在巴西本地制造细胞和基因疗法,针对包括白血病、淋巴瘤和艾滋病毒感染的CAR-T细胞疗法。巴西方面的倡议最初侧重于CAR-T疗法,向巴西公共卫生系统收取每剂约3.5万美元的费用。这大约是美国和欧洲目前批准的CAR-T细胞产品价格的十分之一。同其它模态的药物不同,先进疗法的成本中制造费用占据相当显著的比例。与之形成对比的是,每月价格1000美元左右的Wegovy,其生产成本据称不足5美元,而且最大来源还是注射笔。正是考虑到基因和细胞疗法成本中制造费用的显著贡献,人们才认为在海外生产将大幅降低这些昂贵药物的价格。Caring Cross开发的制造工艺可显著降低制造CAR-T细胞治疗产品的材料成本。这家非营利组织将向Bio-Manguinhos(负责生产疫苗、诊断产品和生物制剂的Fiocruz部门)提供技术、材料和培训,以便其能够生产CAR-T细胞疗法和载体。计划是对实验疗法进行临床试验,然后在巴西寻求批准。Caring Cross方面称,首批研究预计将于今年或2025年初开始,批准的产品可能会在三年内上市。除了材料和培训之外,Caring Cross还将向医院提供专有载体,作为生产和治疗的关键材料。印度的生物技术公司,包括ImmunoACT和Immuneel,正在致力于开发负担得起的CAR-T疗法。即使在欧洲,特殊政策也使得一些医院能够生产自己的CAR-T疗法。据称西班牙巴塞罗那医院诊所开发的一种CAR-T疗法获得了西班牙监管机构的批准,并由国家卫生系统报销,为患者提供了另一种选择,价格为8.9万欧元(9.7万美元),大约是生物制药公司市场上CAR-T产品标价的三分之一。Caring Cross与Fiocruz之间的合作估计将接受2000名患者,每位患者的费用在3.5万到4万美元之间,总成本只有7000万美元,而按照目前的标价则为7亿美元。Caring Cross预计今年到明年开始淋巴瘤和白血病疗法临床试验。这些疗法最初将用于三线治疗,但之后会考虑二线治疗,这将显著扩大应用范围。同印度的合作有所不同,Caring Cross将为ImmunoACT提供载体,后者已经开始销售CAR-T疗法,但已经开始着手下一代产品。ImmunoACT目前以约4万美元的价格出售一种疗法,但只有富人才能负担得起。ImmunoACT希望用Caring Cross材料制成的新疗法能够惠及更多患者。印度目前有大约2.5万到3万人有资格接受ImmunoACT开发的CAR-T产品,但只有2千到5千人能够承担治疗费用。ImmunoACT首席执行官称,目前的计划是向富裕患者收取4万美元,而对其它患者收取3万美元。为了扩大覆盖范围,ImmunoACT希望说服政府提高保险覆盖范围。03影响细胞和基因疗法的长期价值因素细胞和基因疗法的潜在变数包括治疗效果的持久性、特定的患者群体以及替代疗法的可用性,这些都会显著影响成本效益的计算。例如BioMarin的A型血友病基因疗法Roctavian(valoctocogene roxaparvovec)2024年第一季度收获了80万美元的销售额,而BioMarin原本视其为潜在的重磅炸弹。Roctavian针对的是个存在着激烈竞争的市场。患者不仅疗法选择不少,而且价格体系也具有足够的差异性,患者和付款人可能更不愿意尝试新的昂贵的替代方案。替代疗法的可用性,即使效果较差,也将提高新基因疗法的成本效益的门槛高度。随着更多长期数据的出现,细胞和基因疗法是否能够实现其临床承诺,证明其高昂的成本是合理的,将在未来几年变得更加清晰。治疗效果的持久性仍然是一个关键考虑因素。对于先进疗法高价格的一个常见背书是,这些具有终生效果的一次性疗法比需要重复给药的疗法更具成本效益。然而如果这个基础不存在,那么高价便成为了“空中楼阁”。患者群体的规模是另一个重要因素。与更常见疾病的治疗相比,罕见病和超罕见疾病疗法在收回开发成本方面面临着更严峻的挑战,这是由患者群体的数量和可及性决定的。总而言之,先进疗法的推广,需要尽快降低成本,验证其安全性和长期有效性。通过这些手段,这些疗法的市场占有率才能得到显著提升。声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智咨询立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请点击右侧在线咨询反馈。Ref.1.Shah-Neville,W.Can Brazil make cell and gene therapy costs affordable for all?Labiotech.29.04.2024.2.Buntz,B.With prices topping$4 million,high stakes define cell and gene therapy landscape.Drug Discovery&Development.26.04.2024.3.Silverman,E.A nonprofit does deals in Brazil and India to make low-cost CAR-T cell therapies widely available.STAT.08.05.2024.4.Wong,C.H.et al.The estimated annual financial impact of gene therapy in the United States.Gene Ther 30,761–773(2023).https://doi.org/10.1038/s41434-023-00419-9



 产业与战略研究
产业与战略研究 品类与产品规划
品类与产品规划 研发与投资决策
研发与投资决策 卓越上市策划
卓越上市策划 成熟产品策划
成熟产品策划





