近两年,全球有多起核药交易案,总额超百亿美元,诺华、礼来、BMS和阿斯利康等制药巨头纷纷看好这一领域,重金押注。诺华的Pluvicto是目前最成功的RDC药物,在产能受限的2023年销售额近10亿美元,诺华也在马不停蹄的建厂扩产,近期,诺华拟投资6亿元的中国放射性药品生产项目奠基开建,随着产能的上升以及患者的需求,诺华预计Pluvicto峰值能达60亿美元。基于巨大的市场空间,国内外多家药企加入核药的开发,核药正以新的姿态穿越寒冬。近年来,放射性药物(或称“核药”)已成为癌症治疗的一种有前途的方式,其中放射性偶联药物(RDC),即将放射性同位素与包括抗体、多肽或小分子药物进行偶联而得的一类药物,可以将放射性同位素精确靶向递送到癌细胞而备受关注。RDC也是继ADC、GLP-1之后的又一个黄金赛道,引发一众跨国巨头加速布局,如诺华、阿斯利康、礼来和BMS等。今年5月2日,诺华宣布将以首付10亿美元,预定里程碑付款7.5亿美元收购核药初创公司Mariana Oncology,Mariana是一家全面整合的生物技术公司,开创了放射性药物癌症创新疗法的新纪元,利用α和β放射性核素有效载荷从头开始构建具有最佳特性平衡的放射性药物。此次收购将Mariana Oncology的创新放射性药物管线和平台与Novartis久经考验的临床开发和商业化专业技术相结合。Mariana的主要放射配体疗法MC-339,预计将在今年下半年进入小细胞肺癌的人体研究。7月2日,诺华宣布其中国放射性药品生产项目正式启动工程建设,该项目投资总额预计6亿元人民币,这是诺华在中国的首个放射配体疗法生产基地,也是在中国的第二个创新药物生产基地。据介绍,在获得必要监管批准和许可的前提下,诺华中国放射性药品生产项目预计将于2026年底建成投产。阿斯利康也不甘示弱,今年3月19日,阿斯利康宣布将以交易总额约24亿美元收购Fusion Pharmaceuticals,将其一款靶向PSMA(前列腺特异性膜抗原)用于治疗转移性去势抵抗性前列腺癌(mCRPC)的2期临床核心产品FPI-2265收入囊中。FPI-2265递送放射性同位素锕225(225Ac),是一种α放射性药物,与β射线相比,α射线的粒子质量更大,具有更高的效力和更短的射程,靶向α治疗能够实现更高强度的治疗效果且对正常组织的影响范围更小。而礼来在核药领域也动作不断,去年10月礼来宣布以14亿美元收购Point Biopharma,后者的核心产品是放射性药物PNT2002;今年5月,礼来斥资11.6亿美元与Aktis Oncology达成多靶点发现合作协议,利用Aktis的新型微型蛋白技术平台生产肿瘤放射性药物。根据协议,礼来将获得在全球范围内开发由Aktis发现的、针对礼来选定的一系列明确靶标的放射性药物和诊断产品的权利。近日,礼来又宣布与Radionetics Oncology达成最高11.4亿美元的合作协议,推进Radionetics的专有GPCR靶向小分子放射性药物研发进展。BMS也紧追其后,去年12月,BMS以41亿美元的价格收购核药生物技术公司RayzeBio,此次交易将为BMS带来RayzeBio基于α核素的差异化放射性药物平台及多款在研创新产品药物开发项目,包括RYZ101、RYZ801等创新靶向核药,极大丰富了其肿瘤产品管线。RDC是核药领域最具发展潜力的方向之一,是临床实操中唯一能够实现诊疗一体化的药物,可使用相应的药物配合进行治疗,节约时间并提高效率。据不完全统计,自2016年以来,FDA批准了10个RDC上市,包括8款PET诊断药和2款治疗药,目标靶点集中于PSMA和SSTR(生长抑素受体),主要用于前列腺癌(PSMA)和神经内分泌肿瘤(SSTR)的诊断治疗,常用核素分别为68Ga和177Lu(表1)。
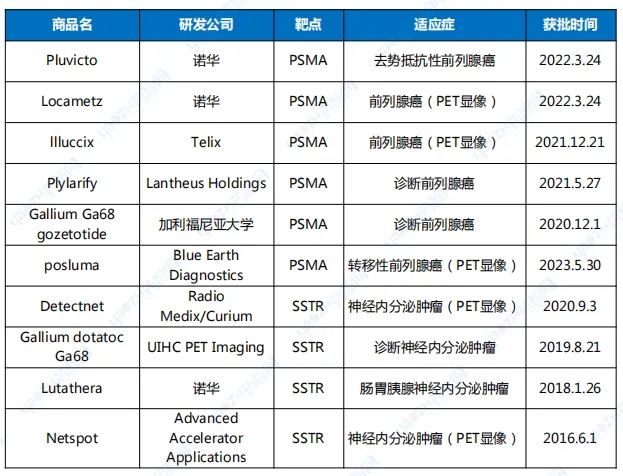
这些上市的RDC治疗药物表现突出的主要为诺华的Lutathera和Pluvicto(177Lu-PSMA-617),其中,Lutathera是全球首款获批上市的放射性配体疗法(RLT),开启了放射性药物靶向治疗新时代,Pluvicto是目前为止年销售额最高的放射性治疗药物,2023年销售总额达9.8亿美元,2024第一季度销售额同比增长47%达到3.10亿美元。Pluvicto是一种靶向PSMA的放射配体疗法,由放射性核素镥-177与PSMA小分子抑制剂PSMA-617连接组成,通过与表达PSMA的细胞结合向表达PSMA的前列腺癌细胞提供辐射,导致随后的细胞因镥-177的β发射而死亡。PSMA是前列腺细胞一类特异性的肿瘤标志物,在大多数前列腺癌组织中高表达,而在正常前列腺组织中低表达,在前列腺癌进展为去势性前列腺癌的过程中,许多前列腺癌细胞可能丢失前列腺特异性抗原,但PSMA仍然得以保留,因此PSMA是一种很有潜力的前列腺癌靶标。2022年3月,Pluvicto获得FDA批准,用于PSMA阳性转移性去势抵抗性前列腺癌三线治疗,虽然针对的是前列腺癌疾病发展的终末阶段mCRPC,但凭借mCRPC拥有较大的患者群体规模以及优异的疗效,3期VISION试验结果显示Pluvicto联合BSoC组的中位OS为15.3个月,显著优于BSoC组的中位OS为11.3个月,Pluvicto自上市以来销售额扶摇直上,今年销售额有望突破10亿美元,跻身重磅炸弹行列(图1)[1,2]。
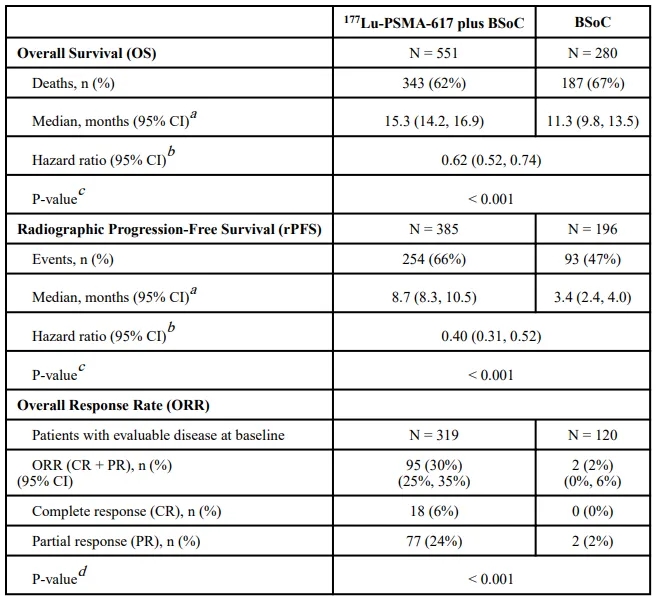
同一天,FDA批准了诺华的一款用于PSMA阳性病变正电子发射断层扫描(PET)的放射性诊断剂Locametz,Locametz是第一个被批准用于使用放射性配体治疗剂的患者选择的放射性诊断剂。除了FDA批准之外,国内也有两款获批的RDC药物,包括先通医药的用于阿尔兹海默症诊断的A-PET显像剂氟[18F]贝他苯注射液以及智核生物的用于无远处转移的分化型甲状腺癌患者在甲状腺全切或近全切除术后碘[131I]清除残余甲状腺组织的辅助治疗的人促甲状腺素注射液(商品名智舒嘉)。国内的核医学起步较晚,先通医药的氟[18F]贝他苯注射液是国内核医学领域近20年首个获批上市的新药,对我国核医学发展有着里程碑般的意义。据不完全统计,全球有数百种临床在研核药产品,其中RDC是重要的一部分,有一百多种诊断和治疗用RDC新药处于临床试验及申请上市阶段,诊断RDC新药常用的核素包括68Ga、99mTc、89Zr等,涉及到的靶点主要包括HER2、FAP-α、PSMA和SSTR等,治疗用RDC新药常用的核素包括177Lu、225Ac、131I、90Y等,针对SSTR/SSTR2、PSMA靶点布局较多,热门适应症包括前列腺癌、神经内分泌肿瘤和白血病等(表2)[3]。
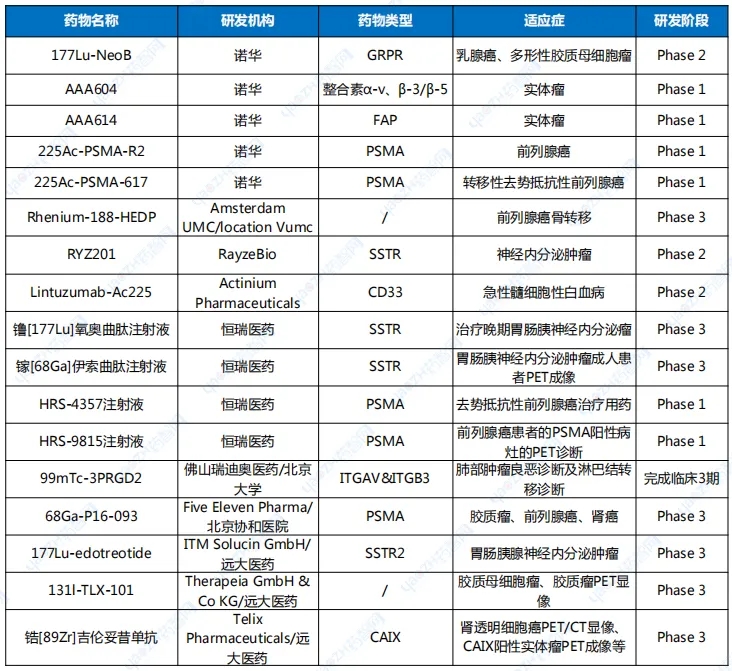
诺华持续深耕核药领域,积极布局多款核药产品,包括靶向GPCR的177Lu-NeoB、靶向整合素α-v、β-3/β-5的AAA604、靶向FAP的AAA614以及靶向PSMA的225Ac-PSMA-R2和225Ac-PSMA-617等。今年4月份,诺华开展了177Lu-NeoB的一项临床1/2a期开放标签、多中心研究,以评估177Lu-NeoB在已知过度表达胃泌素释放肽受体(GRPR)的晚期实体瘤患者中的安全性、耐受性、全身分布、辐射剂量学和抗肿瘤活性。国产药企也在加速这一赛道布局。药智数据显示,中国核药研发企业超过50家,如中国同辐、恒瑞医药、远大医药、东诚药业、原子医学研究院、瑞迪奥科技、智核生物、药明博锐、先通医药等,覆盖放射性元素18F、177Lu、99mTc、68Ga、89Zr、131I等[4]。恒瑞有4款RDC进入临床,包括两款诊断用药镓[68Ga]伊索曲肽注射液、HRS-9815注射液以及2款治疗用药镥[177Lu]氧奥曲肽注射液、HRS-4357注射液。远大医药也有多条诊疗一体化开发开发产品,如TLX591/TLX591CDx、TLX250/TLX250CDx和ITM-11/TOCscan等,智核生物管线中的SNA011和SNA017也是对标诊疗一体化开发。近几年,核药领域非常火热,各大药企纷纷加码,Pluvicto的成功更是点燃了药企研发热情,临床在研核药产品数百条,国内药企研发相对较晚,但是在国内政策支持以及国内研发水平提高的情况下,国产核药创新药将迎头赶上。
参考文献
1.FDA approves Pluvicto for metastatic castration-resistant prostate cancer
2.Jaleh Fallah,et.al,FDA Approval Summary:Lutetium Lu 177 Vipivotide Tetraxetan for Patients with Metastatic Castration-Resistant Prostate Cancer,Clin Cancer Res.2023 May 01;29(9):1651–1657
3.《核药:前世今生、市场规模、准入壁垒、研发热点》,BIG生物创造社
4.《核药风潮席卷!跨国巨头重金布局中国药企如何乘势而上?》,东方财富网
声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智咨询立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请点击右侧在线咨询反馈。
近两年,全球有多起核药交易案,总额超百亿美元,诺华、礼来、BMS和阿斯利康等制药巨头纷纷看好这一领域,重金押注。诺华的Pluvicto是目前最成功的RDC药物,在产能受限的2023年销售额近10亿美元,诺华也在马不停蹄的建厂扩产,近期,诺华拟投资6亿元的中国放射性药品生产项目奠基开建,随着产能的上升以及患者的需求,诺华预计Pluvicto峰值能达60亿美元。基于巨大的市场空间,国内外多家药企加入核药的开发,核药正以新的姿态穿越寒冬。超百亿美元,巨头进军核药近年来,放射性药物(或称“核药”)已成为癌症治疗的一种有前途的方式,其中放射性偶联药物(RDC),即将放射性同位素与包括抗体、多肽或小分子药物进行偶联而得的一类药物,可以将放射性同位素精确靶向递送到癌细胞而备受关注。RDC也是继ADC、GLP-1之后的又一个黄金赛道,引发一众跨国巨头加速布局,如诺华、阿斯利康、礼来和BMS等。今年5月2日,诺华宣布将以首付10亿美元,预定里程碑付款7.5亿美元收购核药初创公司Mariana Oncology,Mariana是一家全面整合的生物技术公司,开创了放射性药物癌症创新疗法的新纪元,利用α和β放射性核素有效载荷从头开始构建具有最佳特性平衡的放射性药物。此次收购将Mariana Oncology的创新放射性药物管线和平台与Novartis久经考验的临床开发和商业化专业技术相结合。Mariana的主要放射配体疗法MC-339,预计将在今年下半年进入小细胞肺癌的人体研究。7月2日,诺华宣布其中国放射性药品生产项目正式启动工程建设,该项目投资总额预计6亿元人民币,这是诺华在中国的首个放射配体疗法生产基地,也是在中国的第二个创新药物生产基地。据介绍,在获得必要监管批准和许可的前提下,诺华中国放射性药品生产项目预计将于2026年底建成投产。阿斯利康也不甘示弱,今年3月19日,阿斯利康宣布将以交易总额约24亿美元收购Fusion Pharmaceuticals,将其一款靶向PSMA(前列腺特异性膜抗原)用于治疗转移性去势抵抗性前列腺癌(mCRPC)的2期临床核心产品FPI-2265收入囊中。FPI-2265递送放射性同位素锕225(225Ac),是一种α放射性药物,与β射线相比,α射线的粒子质量更大,具有更高的效力和更短的射程,靶向α治疗能够实现更高强度的治疗效果且对正常组织的影响范围更小。而礼来在核药领域也动作不断,去年10月礼来宣布以14亿美元收购Point Biopharma,后者的核心产品是放射性药物PNT2002;今年5月,礼来斥资11.6亿美元与Aktis Oncology达成多靶点发现合作协议,利用Aktis的新型微型蛋白技术平台生产肿瘤放射性药物。根据协议,礼来将获得在全球范围内开发由Aktis发现的、针对礼来选定的一系列明确靶标的放射性药物和诊断产品的权利。近日,礼来又宣布与Radionetics Oncology达成最高11.4亿美元的合作协议,推进Radionetics的专有GPCR靶向小分子放射性药物研发进展。BMS也紧追其后,去年12月,BMS以41亿美元的价格收购核药生物技术公司RayzeBio,此次交易将为BMS带来RayzeBio基于α核素的差异化放射性药物平台及多款在研创新产品药物开发项目,包括RYZ101、RYZ801等创新靶向核药,极大丰富了其肿瘤产品管线。全球获批的RDC药物RDC是核药领域最具发展潜力的方向之一,是临床实操中唯一能够实现诊疗一体化的药物,可使用相应的药物配合进行治疗,节约时间并提高效率。据不完全统计,自2016年以来,FDA批准了10个RDC上市,包括8款PET诊断药和2款治疗药,目标靶点集中于PSMA和SSTR(生长抑素受体),主要用于前列腺癌(PSMA)和神经内分泌肿瘤(SSTR)的诊断治疗,常用核素分别为68Ga和177Lu(表1)。表1 自2016年来FDA批准上市的RDC药物数据来源:公开资料整理这些上市的RDC治疗药物表现突出的主要为诺华的Lutathera和Pluvicto(177Lu-PSMA-617),其中,Lutathera是全球首款获批上市的放射性配体疗法(RLT),开启了放射性药物靶向治疗新时代,Pluvicto是目前为止年销售额最高的放射性治疗药物,2023年销售总额达9.8亿美元,2024第一季度销售额同比增长47%达到3.10亿美元。Pluvicto是一种靶向PSMA的放射配体疗法,由放射性核素镥-177与PSMA小分子抑制剂PSMA-617连接组成,通过与表达PSMA的细胞结合向表达PSMA的前列腺癌细胞提供辐射,导致随后的细胞因镥-177的β发射而死亡。PSMA是前列腺细胞一类特异性的肿瘤标志物,在大多数前列腺癌组织中高表达,而在正常前列腺组织中低表达,在前列腺癌进展为去势性前列腺癌的过程中,许多前列腺癌细胞可能丢失前列腺特异性抗原,但PSMA仍然得以保留,因此PSMA是一种很有潜力的前列腺癌靶标。2022年3月,Pluvicto获得FDA批准,用于PSMA阳性转移性去势抵抗性前列腺癌三线治疗,虽然针对的是前列腺癌疾病发展的终末阶段mCRPC,但凭借mCRPC拥有较大的患者群体规模以及优异的疗效,3期VISION试验结果显示Pluvicto联合BSoC组的中位OS为15.3个月,显著优于BSoC组的中位OS为11.3个月,Pluvicto自上市以来销售额扶摇直上,今年销售额有望突破10亿美元,跻身重磅炸弹行列(图1)[1,2]。图1 3期VISION试验结果图片来源:参考文献2同一天,FDA批准了诺华的一款用于PSMA阳性病变正电子发射断层扫描(PET)的放射性诊断剂Locametz,Locametz是第一个被批准用于使用放射性配体治疗剂的患者选择的放射性诊断剂。除了FDA批准之外,国内也有两款获批的RDC药物,包括先通医药的用于阿尔兹海默症诊断的A-PET显像剂氟[18F]贝他苯注射液以及智核生物的用于无远处转移的分化型甲状腺癌患者在甲状腺全切或近全切除术后碘[131I]清除残余甲状腺组织的辅助治疗的人促甲状腺素注射液(商品名智舒嘉)。国内的核医学起步较晚,先通医药的氟[18F]贝他苯注射液是国内核医学领域近20年首个获批上市的新药,对我国核医学发展有着里程碑般的意义。全球在研的核药产品据不完全统计,全球有数百种临床在研核药产品,其中RDC是重要的一部分,有一百多种诊断和治疗用RDC新药处于临床试验及申请上市阶段,诊断RDC新药常用的核素包括68Ga、99mTc、89Zr等,涉及到的靶点主要包括HER2、FAP-α、PSMA和SSTR等,治疗用RDC新药常用的核素包括177Lu、225Ac、131I、90Y等,针对SSTR/SSTR2、PSMA靶点布局较多,热门适应症包括前列腺癌、神经内分泌肿瘤和白血病等(表2)[3]。表2 部分在研的核药产品数据来源:公开资料整理诺华持续深耕核药领域,积极布局多款核药产品,包括靶向GPCR的177Lu-NeoB、靶向整合素α-v、β-3/β-5的AAA604、靶向FAP的AAA614以及靶向PSMA的225Ac-PSMA-R2和225Ac-PSMA-617等。今年4月份,诺华开展了177Lu-NeoB的一项临床1/2a期开放标签、多中心研究,以评估177Lu-NeoB在已知过度表达胃泌素释放肽受体(GRPR)的晚期实体瘤患者中的安全性、耐受性、全身分布、辐射剂量学和抗肿瘤活性。国产药企也在加速这一赛道布局。药智数据显示,中国核药研发企业超过50家,如中国同辐、恒瑞医药、远大医药、东诚药业、原子医学研究院、瑞迪奥科技、智核生物、药明博锐、先通医药等,覆盖放射性元素18F、177Lu、99mTc、68Ga、89Zr、131I等[4]。恒瑞有4款RDC进入临床,包括两款诊断用药镓[68Ga]伊索曲肽注射液、HRS-9815注射液以及2款治疗用药镥[177Lu]氧奥曲肽注射液、HRS-4357注射液。远大医药也有多条诊疗一体化开发开发产品,如TLX591/TLX591CDx、TLX250/TLX250CDx和ITM-11/TOCscan等,智核生物管线中的SNA011和SNA017也是对标诊疗一体化开发。结语近几年,核药领域非常火热,各大药企纷纷加码,Pluvicto的成功更是点燃了药企研发热情,临床在研核药产品数百条,国内药企研发相对较晚,但是在国内政策支持以及国内研发水平提高的情况下,国产核药创新药将迎头赶上。参考文献1.FDA approves Pluvicto for metastatic castration-resistant prostate cancer2.Jaleh Fallah,et.al,FDA Approval Summary:Lutetium Lu 177 Vipivotide Tetraxetan for Patients with Metastatic Castration-Resistant Prostate Cancer,Clin Cancer Res.2023 May 01;29(9):1651–16573.《核药:前世今生、市场规模、准入壁垒、研发热点》,BIG生物创造社4.《核药风潮席卷!跨国巨头重金布局中国药企如何乘势而上?》,东方财富网声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智咨询立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请点击右侧在线咨询反馈。



 产业与战略研究
产业与战略研究 品类与产品规划
品类与产品规划 研发与投资决策
研发与投资决策 卓越上市策划
卓越上市策划 成熟产品策划
成熟产品策划





