今年,代谢功能障碍相关性脂肪性肝炎(MASH,曾称为NASH)领域迎来了一系列变化。
3月,美国FDA批准了全球首款MASH疗法Rezdiffra上市,来自Madrigal Pharmaceuticals公司。随后又有多家公司公布了其潜在MASH候选药物的最新数据,希望能够与Madrigal一较高下,例如Viking Therapeutics公司的VK2809,Sagimet Biosciences公司的denifanstat等。但也有公司在考虑了临床前数据后,放弃了部分MASH管线。
MASH是一种与代谢紊乱相关的肝脏疾病,早前曾被称为非酒精性脂肪性肝炎(NASH)。该病症属于代谢相关脂肪性肝病(MAFLD)的一种严重形式,与2型糖尿病、高血压和高血脂等代谢综合征及肥胖等因素密切相关。MASH患者肝脏中脂肪积聚过多,并伴随炎症和肝细胞损伤。这种炎症和损伤最终可能导致肝纤维化、肝硬化、肝衰竭甚至肝死亡。
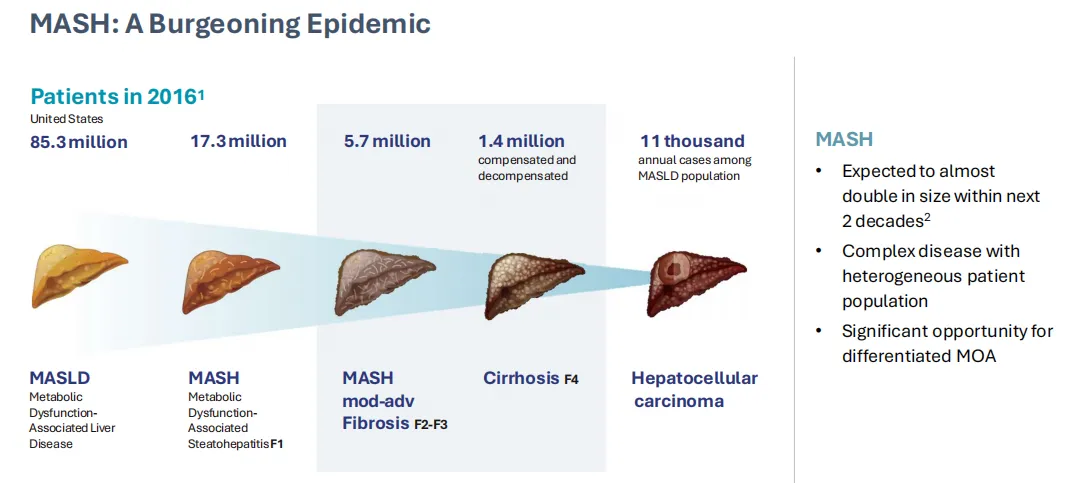
图片来源:参考资料2
MASH的患者基数庞大,而且随着肥胖率的上升,全球患病率或将继续上涨。根据弗若斯特沙利文,到2025年全球MASH药物市场将达到107亿美元,并于2030年达到322亿美元。
然而,MASH目前治疗方法非常有限,今年3月才迎来首个治疗新药。
2024年3月,Madrigal Pharmaceuticals开发的甲状腺激素受体-β(THR-β)激动剂resmetirom(商品名:Rezdiffra)获得美国FDA批准上市,联合饮食和运动治疗成人非肝硬化非酒精性脂肪性肝炎患有中度至晚期肝纤维化(与F2至F3纤维化阶段一致)。该药成为第一个也是唯一一个获得FDA批准用于治疗MASH的药物。
该药其核心作用机制在于其对肝脏内THR-β的激活。甲状腺激素在调节新陈代谢、改善胰岛素敏感性以及降低血脂水平等方面起着关键作用。通过选择性激活THR-β,resmetirom能够促进肝脏对脂肪酸的代谢,减少脂肪在肝脏中的积累,减少肝脏中的炎症反应和纤维化过程。
其批准是基于MAESTRO-NASH试验结果。该试验达到了两项主要终点及多个次要终点。
数据显示,在第52周时,分别有25.9%与29.9%的80 mg、100 mg resmetirom组患者实现NASH症状消除且肝纤维化未恶化,而安慰剂组中这一比例为9.7%(P<0.001)。此外,80 mg与100 mg resmetirom组患者分别有24.2%与25.9%实现了纤维化至少一个阶段的改善且NAFLD活动评分没有恶化,相较之下安慰剂组患者在此数值的比率仅有14.2%(P<0.001)。而且resmetirom在两种剂量下均表现出良好的安全性和耐受性。
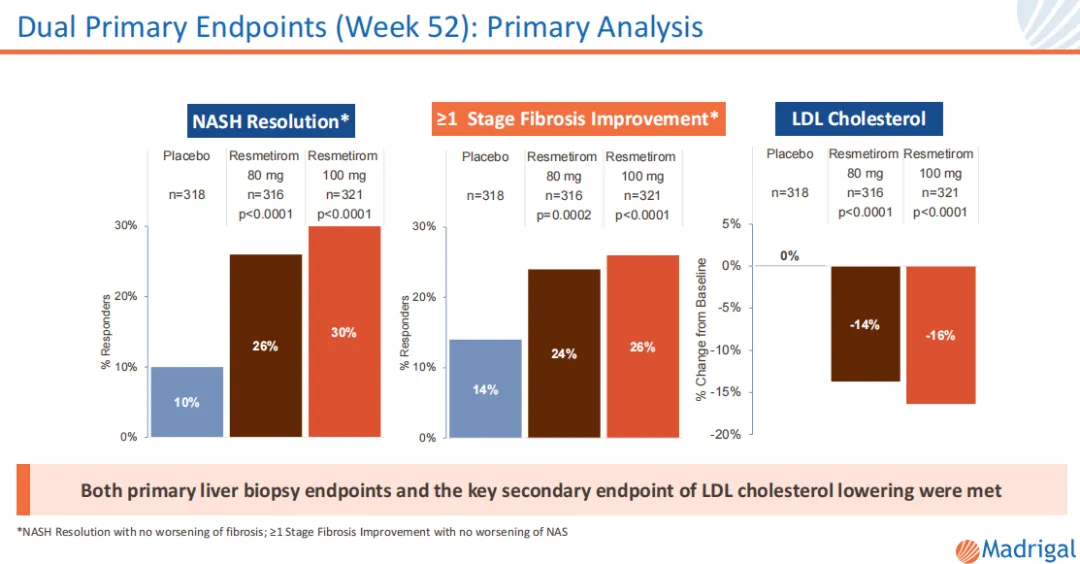
图片来源:Madrigal官网
据Madrigal Pharmaceuticals公司2024年第二季度财报,resmetirom上市后首个季度实现销售额1460万美元。
Resmetirom的获批为MASH患者的治疗提供了新手段,也证明了THR-β激动剂路线的可行性。
而紧随其后的还有多个THR-β激动剂在最近公布了最新临床数据,希望与其一较高下。
Viking公司的VK2809是另一款备受期待的THR-β激动剂。
VK2809是一款新型肝脏选择性甲状腺受体β亚型(TRβ)激动剂,对肝组织和β受体亚型具有选择性。
今年6月,Viking公布了VK2809在2b期VOYAGE研究的52周组织学积极数据。
>>主要终点:接受VK2809治疗的患者在第12周时肝脏脂肪含量显著减少,而且在第52周时继续表现出肝脏脂肪含量显著减少,与基线相比的平均相对变化范围为37%至55%。10mg组应答率(定义为肝脏脂肪减少≥30%的患者比例)高达88%。
>>次要终点:52周时,在NASH缓解且纤维化未恶化方面,接受VK2809治疗患者的NASH缓解率为63%至75%,而此数值在安慰剂组患者仅为29%。在纤维化改善且NASH无恶化方面,接受VK2809治疗患者的纤维化改善率在44%至57%之间,而此数值在安慰剂组患者仅为34%。
>>VK2809在52周的治疗中表现出令人鼓舞的安全性和耐受性。
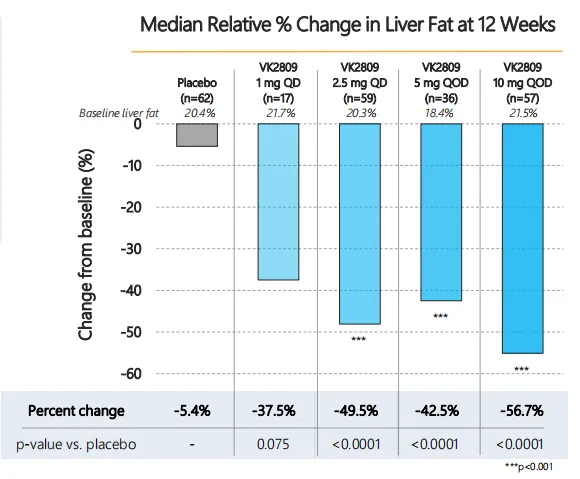
图片来源:Viking官网
除了Viking,Aligos Therapeutics公司也传来喜报。
其THR-β激动剂ALG-055009在MASH患者中的2a期HERALD研究结果积极。ALG-055009不仅有可能改善MASH的分辨率,还可能改善纤维化。
结果显示:经过12周治疗,安慰剂调整后,患者经MRI-PDFF评估的中位肝脂肪相对减少量达46.2%。与基线相比,多达70%的受试者其肝脏脂肪相对减少量达到≥30%。
从目前数据来看,无论是VK2809,还是ALG-055009与resmetirom相比似乎都更有利,但都还需要更多的临床数据来证明其BIC属性。
此外,国内药企也有众多布局THR-β激动剂,如歌礼制药的ASC41、海思科的HSK31679、拓臻生物的TERN-501、诚益生物的ECC4703都已进入临床阶段。
然而,从上文也可以看到,并非所有患者都对THR-β激动剂有反应。MASH发病机制复杂,还需要开发其他靶点的新药来治疗更多患者。
目前在研的治疗方案除了THR-β激动剂,还有脂肪酸合成酶抑制剂、胰高血糖素样肽-1受体(GLP-1R)激动剂、FGF类似物几大类。
Sagimet Biosciences公司的denifanstat(ASC40)是一款脂肪酸合成酶抑制剂。其治疗MASH的2b期临床试验FASCINATE-2的结果显示,denifanstat在疾病活动、MASH缓解和肝纤维化方面均实现了具有统计学显著性和临床意义的改善,支持这一疗法进入3期临床试验。
数据显示,在第52周,36%的denifanstat组患者达成MASH缓解且不伴肝纤维化恶化,并且非酒精性脂肪肝活动评分(NAS)降低≥2分,与之相比,安慰剂组这一数值仅为13%(p=0.002)。此外,有52%的denifanstat组患者的NAS降低≥2分且无肝纤维化恶化,安慰剂组患者这一数值为20%(p=0.0001)。
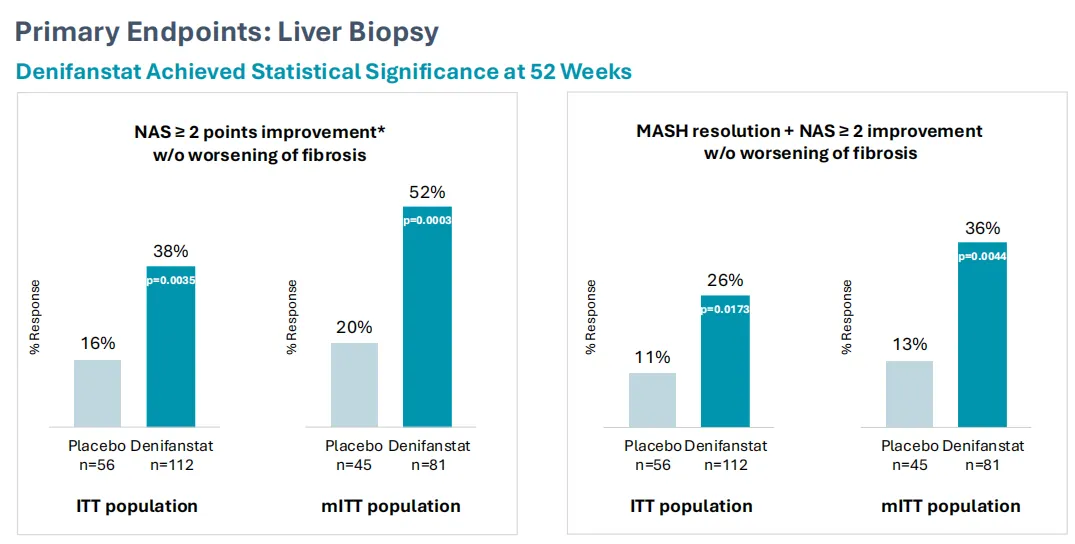
图片来源:参考资料2
安全性方面,未观察到与治疗相关的严重不良事件(SAEs),大多数不良事件(AEs)为轻度至中度(1级和2级)。
值得一提的是,歌礼已从Sagimet获得ASC40的大中华区独家授权。
胰高血糖素样肽-1受体(GLP-1R)激动剂是基于肠促胰素的降糖药物,具有增加胰岛素敏感性、减少脂质积累、改善肝线粒体功能和抑制受损ER的应激反应等机制从而发挥保肝作用。
目前,诺和诺德的司美格鲁肽进展最快,已处于临床Ⅲ期。其Ⅱ期临床NN9931-4296研究结果显示,经72周治疗,高、中、低剂量组MASH病理消退且肝纤维化未进展的患者比例为59%、36%、40%,而安慰剂发生率为17%,达到主要终点。但该药在纤维化改善方面存疑。司美格鲁肽治疗MASH的效果还需要更大型的临床研究来验证。
礼来的GIP/GLP-1受体双重激动剂替尔泊肽表现似乎更为亮眼。其II期SYNERGY-NASH研究数据显示,与安慰剂相比,73.3%接受最高剂量Tirzepatide治疗患者实现MASH消退且肝纤维化未恶化此主要终点,且过半患者产生≥1级肝纤维化显著改善。
此外,礼来的GCGR/GIPR/GLP-1R三重激动剂retatrutide,BI的GCGR/GLP-1R双靶点激动剂survodutide也展现出了治疗MASH的潜力,不过都还要等待Ⅲ期临床的验证。
FGF21是FGF超家族的非典型成员,在调节能量平衡以及葡萄糖和脂质平衡方面发挥着重要作用。
目前,Akero开发的efruxifermin是首个进入Ⅲ期临床试验的FGF21类似物,在MASH领域展现出了积极的疗效。
其治疗MASH(F2-F3)IIb期HARMONY研究显示,第24周时,每周一次皮下注射Efruxifermin 28mg和50mg剂量组均达到了改善肝脏纤维化的主要终点,分别有39%和41%的患者实现了纤维化改善≥1级且MASH没有恶化,而安慰剂组为20%。96周时,Efruxifermin 50mg组纤维化改善≥1且MASH没有恶化患者比例增至75%,28mg组增至46%,而安慰剂为24%。
其他机制的在研MASH疗法还有线粒体解偶联剂、ASO疗法、Gal-3抑制剂、CCR2/CCR5抑制剂、ASK1抑制剂,以及针对多个靶点的联合疗法等。
NASH发病机制复杂,过去由于对该疾病认知不足,曾有多个药物折戟,被称为“研发黑洞”。但2023年该疾病改名为MASH,意味着人们对该疾病有了更深刻的认知。而今年,Rezdiffra成为第一个获得FDA批准用于治疗该病症的药物,MASH领域迎来了重大改变。
但是新药研发总是失败者众,成功者寡。
此前,默沙东、诺华、强生、BMS等制药巨头都曾折戟MASH赛道。近日,吉利德宣布终止与韩国生物技术公司Yuhan的一项价值7.85亿美元的合作。该合作针对两种MASH疗法权益,终止原因是,在最终候选药物选择阶段,临床前数据不足或最终难以说服吉利德留下相应权利。
MASH复杂的发病机制使其治疗药物开发充满挑战。而且MASH或许本质上不是同一种疾病,不同患者虽然病理切片看起来一样,但他们可能由不同的致病机制驱动。未来,针对不同的发病原因,可能将有更多创新疗法被开发用于治疗MASH。
1.https://www.fiercebiotech.com/biotech/gilead-gives-15m-mash-bet-yuhan-after-mulling-preclinical-data2.https://ir.sagimet.com/static-files/df000576-3450-4a62-9b8a-2ce2bea46f943.MASH突破性疗法ASC40(地尼法司他)最新结果登《柳叶刀》子刊歌礼拥有大中华区权益4.Life Metabolism综述|代谢功能障碍相关脂肪性肝炎(MASH)的临床治疗策略及新型疗法
声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智咨询立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请点击右侧在线咨询反馈。
今年,代谢功能障碍相关性脂肪性肝炎(MASH,曾称为NASH)领域迎来了一系列变化。3月,美国FDA批准了全球首款MASH疗法Rezdiffra上市,来自Madrigal Pharmaceuticals公司。随后又有多家公司公布了其潜在MASH候选药物的最新数据,希望能够与Madrigal一较高下,例如Viking Therapeutics公司的VK2809,Sagimet Biosciences公司的denifanstat等。但也有公司在考虑了临床前数据后,放弃了部分MASH管线。01百亿美元市场MASH是一种与代谢紊乱相关的肝脏疾病,早前曾被称为非酒精性脂肪性肝炎(NASH)。该病症属于代谢相关脂肪性肝病(MAFLD)的一种严重形式,与2型糖尿病、高血压和高血脂等代谢综合征及肥胖等因素密切相关。MASH患者肝脏中脂肪积聚过多,并伴随炎症和肝细胞损伤。这种炎症和损伤最终可能导致肝纤维化、肝硬化、肝衰竭甚至肝死亡。图片来源:参考资料2MASH的患者基数庞大,而且随着肥胖率的上升,全球患病率或将继续上涨。根据弗若斯特沙利文,到2025年全球MASH药物市场将达到107亿美元,并于2030年达到322亿美元。然而,MASH目前治疗方法非常有限,今年3月才迎来首个治疗新药。2024年3月,Madrigal Pharmaceuticals开发的甲状腺激素受体-β(THR-β)激动剂resmetirom(商品名:Rezdiffra)获得美国FDA批准上市,联合饮食和运动治疗成人非肝硬化非酒精性脂肪性肝炎患有中度至晚期肝纤维化(与F2至F3纤维化阶段一致)。该药成为第一个也是唯一一个获得FDA批准用于治疗MASH的药物。该药其核心作用机制在于其对肝脏内THR-β的激活。甲状腺激素在调节新陈代谢、改善胰岛素敏感性以及降低血脂水平等方面起着关键作用。通过选择性激活THR-β,resmetirom能够促进肝脏对脂肪酸的代谢,减少脂肪在肝脏中的积累,减少肝脏中的炎症反应和纤维化过程。其批准是基于MAESTRO-NASH试验结果。该试验达到了两项主要终点及多个次要终点。数据显示,在第52周时,分别有25.9%与29.9%的80 mg、100 mg resmetirom组患者实现NASH症状消除且肝纤维化未恶化,而安慰剂组中这一比例为9.7%(P<0.001)。此外,80 mg与100 mg resmetirom组患者分别有24.2%与25.9%实现了纤维化至少一个阶段的改善且NAFLD活动评分没有恶化,相较之下安慰剂组患者在此数值的比率仅有14.2%(P<0.001)。而且resmetirom在两种剂量下均表现出良好的安全性和耐受性。图片来源:Madrigal官网据Madrigal Pharmaceuticals公司2024年第二季度财报,resmetirom上市后首个季度实现销售额1460万美元。02Resmetirom挑战者众多Resmetirom的获批为MASH患者的治疗提供了新手段,也证明了THR-β激动剂路线的可行性。而紧随其后的还有多个THR-β激动剂在最近公布了最新临床数据,希望与其一较高下。Viking公司的VK2809是另一款备受期待的THR-β激动剂。VK2809是一款新型肝脏选择性甲状腺受体β亚型(TRβ)激动剂,对肝组织和β受体亚型具有选择性。今年6月,Viking公布了VK2809在2b期VOYAGE研究的52周组织学积极数据。>>主要终点:接受VK2809治疗的患者在第12周时肝脏脂肪含量显著减少,而且在第52周时继续表现出肝脏脂肪含量显著减少,与基线相比的平均相对变化范围为37%至55%。10mg组应答率(定义为肝脏脂肪减少≥30%的患者比例)高达88%。>>次要终点:52周时,在NASH缓解且纤维化未恶化方面,接受VK2809治疗患者的NASH缓解率为63%至75%,而此数值在安慰剂组患者仅为29%。在纤维化改善且NASH无恶化方面,接受VK2809治疗患者的纤维化改善率在44%至57%之间,而此数值在安慰剂组患者仅为34%。>>VK2809在52周的治疗中表现出令人鼓舞的安全性和耐受性。图片来源:Viking官网除了Viking,Aligos Therapeutics公司也传来喜报。其THR-β激动剂ALG-055009在MASH患者中的2a期HERALD研究结果积极。ALG-055009不仅有可能改善MASH的分辨率,还可能改善纤维化。结果显示:经过12周治疗,安慰剂调整后,患者经MRI-PDFF评估的中位肝脂肪相对减少量达46.2%。与基线相比,多达70%的受试者其肝脏脂肪相对减少量达到≥30%。从目前数据来看,无论是VK2809,还是ALG-055009与resmetirom相比似乎都更有利,但都还需要更多的临床数据来证明其BIC属性。此外,国内药企也有众多布局THR-β激动剂,如歌礼制药的ASC41、海思科的HSK31679、拓臻生物的TERN-501、诚益生物的ECC4703都已进入临床阶段。03发病机制复杂,需要更多“解药”然而,从上文也可以看到,并非所有患者都对THR-β激动剂有反应。MASH发病机制复杂,还需要开发其他靶点的新药来治疗更多患者。目前在研的治疗方案除了THR-β激动剂,还有脂肪酸合成酶抑制剂、胰高血糖素样肽-1受体(GLP-1R)激动剂、FGF类似物几大类。脂肪酸合成酶抑制剂Sagimet Biosciences公司的denifanstat(ASC40)是一款脂肪酸合成酶抑制剂。其治疗MASH的2b期临床试验FASCINATE-2的结果显示,denifanstat在疾病活动、MASH缓解和肝纤维化方面均实现了具有统计学显著性和临床意义的改善,支持这一疗法进入3期临床试验。数据显示,在第52周,36%的denifanstat组患者达成MASH缓解且不伴肝纤维化恶化,并且非酒精性脂肪肝活动评分(NAS)降低≥2分,与之相比,安慰剂组这一数值仅为13%(p=0.002)。此外,有52%的denifanstat组患者的NAS降低≥2分且无肝纤维化恶化,安慰剂组患者这一数值为20%(p=0.0001)。图片来源:参考资料2安全性方面,未观察到与治疗相关的严重不良事件(SAEs),大多数不良事件(AEs)为轻度至中度(1级和2级)。值得一提的是,歌礼已从Sagimet获得ASC40的大中华区独家授权。GLP-1R激动剂胰高血糖素样肽-1受体(GLP-1R)激动剂是基于肠促胰素的降糖药物,具有增加胰岛素敏感性、减少脂质积累、改善肝线粒体功能和抑制受损ER的应激反应等机制从而发挥保肝作用。目前,诺和诺德的司美格鲁肽进展最快,已处于临床Ⅲ期。其Ⅱ期临床NN9931-4296研究结果显示,经72周治疗,高、中、低剂量组MASH病理消退且肝纤维化未进展的患者比例为59%、36%、40%,而安慰剂发生率为17%,达到主要终点。但该药在纤维化改善方面存疑。司美格鲁肽治疗MASH的效果还需要更大型的临床研究来验证。礼来的GIP/GLP-1受体双重激动剂替尔泊肽表现似乎更为亮眼。其II期SYNERGY-NASH研究数据显示,与安慰剂相比,73.3%接受最高剂量Tirzepatide治疗患者实现MASH消退且肝纤维化未恶化此主要终点,且过半患者产生≥1级肝纤维化显著改善。此外,礼来的GCGR/GIPR/GLP-1R三重激动剂retatrutide,BI的GCGR/GLP-1R双靶点激动剂survodutide也展现出了治疗MASH的潜力,不过都还要等待Ⅲ期临床的验证。FGF类似物FGF21是FGF超家族的非典型成员,在调节能量平衡以及葡萄糖和脂质平衡方面发挥着重要作用。目前,Akero开发的efruxifermin是首个进入Ⅲ期临床试验的FGF21类似物,在MASH领域展现出了积极的疗效。其治疗MASH(F2-F3)IIb期HARMONY研究显示,第24周时,每周一次皮下注射Efruxifermin 28mg和50mg剂量组均达到了改善肝脏纤维化的主要终点,分别有39%和41%的患者实现了纤维化改善≥1级且MASH没有恶化,而安慰剂组为20%。96周时,Efruxifermin 50mg组纤维化改善≥1且MASH没有恶化患者比例增至75%,28mg组增至46%,而安慰剂为24%。其他机制的在研MASH疗法还有线粒体解偶联剂、ASO疗法、Gal-3抑制剂、CCR2/CCR5抑制剂、ASK1抑制剂,以及针对多个靶点的联合疗法等。04结语NASH发病机制复杂,过去由于对该疾病认知不足,曾有多个药物折戟,被称为“研发黑洞”。但2023年该疾病改名为MASH,意味着人们对该疾病有了更深刻的认知。而今年,Rezdiffra成为第一个获得FDA批准用于治疗该病症的药物,MASH领域迎来了重大改变。但是新药研发总是失败者众,成功者寡。此前,默沙东、诺华、强生、BMS等制药巨头都曾折戟MASH赛道。近日,吉利德宣布终止与韩国生物技术公司Yuhan的一项价值7.85亿美元的合作。该合作针对两种MASH疗法权益,终止原因是,在最终候选药物选择阶段,临床前数据不足或最终难以说服吉利德留下相应权利。MASH复杂的发病机制使其治疗药物开发充满挑战。而且MASH或许本质上不是同一种疾病,不同患者虽然病理切片看起来一样,但他们可能由不同的致病机制驱动。未来,针对不同的发病原因,可能将有更多创新疗法被开发用于治疗MASH。参考资料:1.https://www.fiercebiotech.com/biotech/gilead-gives-15m-mash-bet-yuhan-after-mulling-preclinical-data2.https://ir.sagimet.com/static-files/df000576-3450-4a62-9b8a-2ce2bea46f943.MASH突破性疗法ASC40(地尼法司他)最新结果登《柳叶刀》子刊歌礼拥有大中华区权益4.Life Metabolism综述|代谢功能障碍相关脂肪性肝炎(MASH)的临床治疗策略及新型疗法声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智咨询立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请点击右侧在线咨询反馈。




 产业与战略研究
产业与战略研究 品类与产品规划
品类与产品规划 研发与投资决策
研发与投资决策 卓越上市策划
卓越上市策划 成熟产品策划
成熟产品策划





